Topics
2020.09.30 circular No.15
個性のある研究をすることの難しさ東京農工大学名誉教授、特別招聘教授
大野 弘幸
軽快なピアノトリオの曲を聞くと、「ああ、これはモーツァルトだな」と感じる。ひまわりの絵を見ると、「これはゴッホの作品だ」と分かる。このように、作品に接すると作者がすぐに分かる芸術家は、岡本太郎や桑田佳祐など、日本にもたくさんいる。作品に接して作者がすぐに思い浮かぶと言うことは素晴らしいことだ。私は2020年3月末日を持って東京農工大学を定年退官したが、現役の教員の間、研究発表や論文を見て、「この研究は○○さんの仕事だな。」と分かるような研究をしたいと思っていた。研究室の博士課程の学生を相手に、赤ワインを飲みながら、こんな研究をしたいなぁと常々話していた。しかし、実践するとなるととても難しいものだ。私が学生諸君と行ってきた研究はどうだったのだろうかと思い出しながら、20年以上にわたるイオン液体研究と、そこに至るまでの研究を振り返ってみたいと思う。
2. ポリエーテルとの出会い
3. アメリカでプロテオグリカンと出会う
早稲田大学の博士課程の学生だった頃、リン脂質が自己集合して形成するリポソームと水溶性高分子の相互作用を研究していた。ポリエチレンオキシド(PEO)は当時細胞融合を引き起こすことが知られており、そのモデルとしてリポソームとの相互作用を調べていた。電荷を持つ高分子はリン脂質と強く相互作用するが、電荷を持たないノニオン性高分子も相互作用し、リン脂質の膜流動性を低下させる。PEO は特にリン脂質の親水部であるコリン基と強く相互作用し、そのメチルプロトンの運動性を低下させた1。今から思えば、リン脂質の構造や相互作用などを1970年代の終わり頃に勉強していたのが後日大変役に立った。また、ヒト赤血球の融合を誘発する能力の評価に使っていたPEO誘導体の中に、長鎖脂肪酸とPEOのエステルがあった2。このエステルを利用しているうちに、PEO末端のヒドロキシル基を様々に修飾する方法を学んだ。これが後日、PEO-塩ハイブリッドの設計につながることになる。赤血球膜とPEOの相互作用を解析するために、脂質の運動性を蛍光偏向解消法で追跡した3のもこの頃で、後の導波路分光法を基板上のタンパク質の解析に使った起源がこの辺にあるようだ。
一方、修士課程のテーマであったポリマーコンプレックスの研究も継続しており、静電相互作用を介するポリイオンコンプレックスのみならず、水素結合などを介するポリマーコンプレックスも対象にしていた。1981年には多糖類とPEOなどの水溶性高分子とのコンプレックス形成を報告した4。ポリマーコンプレックスを形成させるときは、それぞれの成分高分子を水溶液とし、これを混合させるが、コンプレックス形成の初期過程は水と高分子のどちらがより強く相互作用するのかと言う競争反応になる。これには水素結合力の差異が大きく反映される。また、含水率はコンプレックスの物性に大きく影響するので、脱水和を調べることは高分子間の相互作用力の指標が得られると考え、形成後のコンプレックス内部の結合水の研究も行った。実際の含水量を徐々に減らし、DSC測定で系に含まれる水の融解に伴う熱エネルギーを解析すると、含水量がゼロになる前に熱エネルギーがゼロになる。これが結合水、特に不凍水と呼ばれる強く結合している水分子の量を反映していることになる5。この頃の結合水の議論が30年後の水和イオン液体の議論に生きてくる。
また、PEOに塩を添加したものがイオン伝導体になることはWrightが1973年に報告していた。イオン伝導にも興味があったので、PEOよりも極性の強いポリヒニリデンフルオライド(PVdF)に極性有機溶媒とリチウム塩を加えて、イオン伝導性フィルムを作成すると、室温で10-5S/cm 程度のイオン伝導度が得られた6。固体の中をイオンが動くためにはガラス転移温度が低くないとダメだが、そんなポリマーは決して多くはない。他の分子と相互作用する(いわゆる機能発現する)ということは、ガラス転移温度を上昇させてしまうことをいやと言うほど感じた。この頃、イオン伝導度の測定法やArrhenius Plot を使ったデータ処理を経験しているのも、後日役立った。更に、末端にカルボキシル基を導入したPEOをポリメタクリル酸に付けた櫛形ポリマーを使い、種々のアルカリ金属塩を添加し、それらのアルカリ金属イオンの移動を解析したところ、高分子固体中でも大きなセシウムカチオンなどの方がリチウムイオンよりも速く動けることを実証した7。
1981年3月に博士学位を取得し、2年間早稲田大学で研究員として自由に研究を楽しんだ後、1983年4月から2年間、米国オハイオ州クリーブランドにある Case Western Reserve University にポスドクとして勤務した。当時、高分子研究に関わる多くの研究者が集まっていたので、この大学でのポスドクを希望した。私のボスのBlackwell教授が獲得してきたグラントのテーマのひとつが「プロテオグリカン類の構造と老化の相関」であり、その経費で私が雇われたことになる。ヒヨコから抽出されたプロテオグリカンを生物学教室から貰ってきて、その構造を動的光散乱法や透過型電子顕微鏡で解析すると言う日々だった。全く新しい材料を新しい方法論で解析するのはスタートこそ大変だったが、毎日新しい発見があり、いろいろな人に助けられて面白くなっていった。Zimm Plot や排除体積効果なども身近になった。Blackwell教授の研究室では、色々な多糖類や天然高分子が作る高次構造を研究しており、メンバーとの議論は面白かった。研究もそこそこ行ったが、ビールを触媒としてラボのメンバーと懇親を深めたことや、週末のドライブの方が記憶に残っている。
4. 高分子化リポソームで個性を出す
1985年に早稲田に戻り、直ぐに渡米前のテーマに関わることになった。助手となり自由度も増えたので、ビニル基を導入したリン脂質を使ってリポソームを形成させ、重合して丈夫なマイクロカプセルを作ろうとした。しかし、既に高分子化リポソームの研究はなされており、独創的な研究にはつながらないと思ったので、重合性リン脂質と一般の膜成分(天然リン脂質やコレステロール)を混合し、リポソームを形成させてから、膜上で相分離させ、それを重合して固定しようとした。膜強度を改善することなど全く考えずに、面白そうだからと言う理由で実験をした。当時4年生だった武岡真司君(早稲田大学教授)と一緒に実験し、重合後、非重合成分を洗い流し、高分子化されたリポソームの走査型電子顕微鏡写真を撮り続けていたが、ついに穴の開いた高分子化リポソームを写真にとることに成功した。3D感を出すために、僅かに角度を変えてSEM写真を撮り、立体写真とした(図1)。早速論文8にしたが、その時のタイトルは単語がわずか3つ。「Skeletonized hybrid liposomes」というタイトルは実験中から考えていたもので、この頃から「面白い研究」もアリだなと考えるようになった。応用は他の人が考えればよく、科学的に興味のあることをしてみようと強く思った。
リポソームの高分子化研究はさらに進み、親水部近くの2,4位にジエン基を持つアシル鎖2本からなるフォスフォリルコリン型リン脂質を日油㈱の研究所の方々に作ってもらい、それを使ってリポソームを形成させ、水溶性と脂溶性の重合開始剤を使い分けて、重合過程を追跡した。2つのアシル鎖のジエン基の環境が異なることを重合度から議論できた。1-アシル鎖のジエン基は脂溶性の重合開始剤(AIBN)で重合が進み、2-アシル鎖のジエン基は水溶性の重合開始剤で重合が進むこと、さらには1-アシル鎖のジエン基と2-アシル鎖のジエン基は共重合しないことなどを明らかにした9。その後もリポソームの高分子化では面白い成果をいくつか出すことができた。
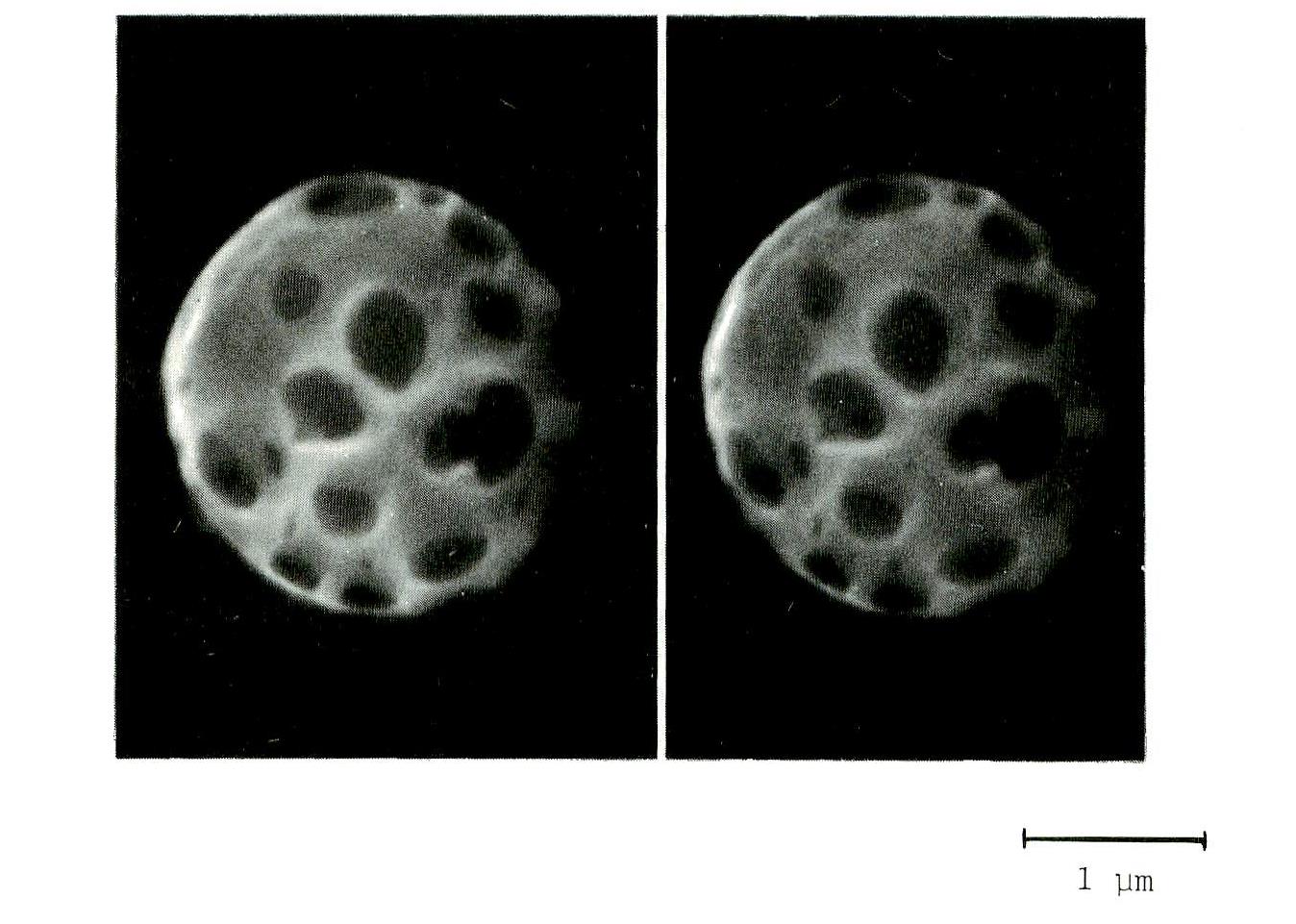
図1. スケルトン化した高分子化リポソーム
5. 農工大で新しく研究をスタートするも研究資金無し
1988年8月に東京農工大学工学部に助教授として着任し、「さあ個性のある研究をするぞ!」と意気込んだが、装置も試薬も無い所ではそうもいかない。夏に着任したが、早速、来年度に大学院への進学が決定した3人の4年生が研究室に配属となり、彼らを半年間で卒業させなくてはならなくなった。その上、退官した教授が残していった実験器具類などが漠然と置かれた実験室を貰ったので、毎日実験室の掃除と片付けで、研究生活とはとても言えない状況だった。毎日掃除をしながら、研究費が無ければ研究ができないということをいやというほど感じた。当時は研究のスタートアップ資金制度など無く、大学は当然のこと、学部も学科も全く支援してくれなかった。そのため若手の教員は教授と組んで講座制を運営するのが通常であったが、敢えて半講座制で独立を希望した。しかし背に腹は替えられず、大学に研究費を借金すると共に、科研費をはじめ、財団の研究支援に必死で申し込んだ。
6. 動的イオン伝導度測定装置
借金で装置や試薬を購入し、3人の第1期生が卒業論文を何とか提出できるところまでやり、大学院に進学したと思ったら、第2期生が入ってきた。研究の柱を立てるために、サンプルを加熱しながらイオン伝導度を連続的に測定し、アレニウスプロットを30分程度で描くことのできるシステムを作り上げることにした。このテーマは第1期生の笹山洋行君の修士論文のテーマだ。彼はPC9801 を駆使して幅広い周波数帯でインピーダンス測定を瞬時に行うプログラムの作成から、温度センサーとペルチェ素子で囲まれた電極セルの作成まで基礎を確立してくれた。その後、何人かの学生によって数回にわたり改善が加わったものの、当時、インピーダンス測定のプロットだけで連続したアレニウスカーブが得られたのは我々の研究室だけだった。通常のサンプルのイオン伝導度のアレニウスプロットを短時間で得られるのはもちろんのこと、相転移を示すような材料のイオン伝導度についても、温度変化に応じてジャンプする様子の動的測定にも威力を発揮した(図2)10。ペルチェ素子を使っているため、昇温のみならず定速降温測定もできたのでヒステリシスを示す系の観測もできた。このシステムを駆使して様々な材料のイオン伝導度の動的測定を実施し、たくさんの論文を執筆できた。
横道にそれるが、分子量の異なるPEOと無機塩の混合物の研究をしていたところ、PEOオリゴマーに種々の無機塩を溶解させて、加熱すると溶解度が低下するものが見つかった11,12。温めると溶けにくくなる溶液との付き合いがこの頃始まった。
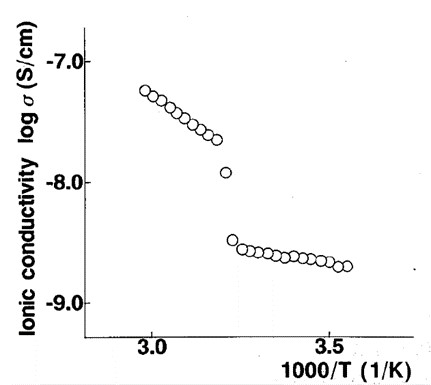
図2. 側鎖にPEOを有するくし型ポリマーに塩を加えた系のイオン伝導度のアレニウスプロット
7. PEO-修飾タンパク質
PEO誘導体に興味を持ち、周辺を調べてみると、既に末端にカルボキシル基を有するPEOなどは市販されていたが、これらは主にタンパク質のPEO修飾に使われるような状況だった。当時は生体適合性を付与させるためにPEO修飾が様々な物質に施されていた。PEOそのものが高分子溶媒(物理学的に矛盾する言葉だが)として眺められることを記事にした13が、その流れでPEO中にタンパク質を溶かすためにはPEO修飾が有効だった。たとえばヘムタンパクの一種であるシトクロムcをPEO修飾し、支持塩を溶かしたPEOに溶解させると、電気化学的に酸化還元させることができた14。PEO中のタンパク質の電気化学は、1990年から研究室メンバーとなった文部技官の山口夏江さん (長岡技科大)が中心になって推進していた。彼女は、PEO修飾ヘモグロビンがPEO中では120℃でもその酸化還元活性を示すことを初めて観測し15、もはやタンパク質は扱いずらいものではなく、デバイスとして使えると息巻いた。当時はタンパク質を分子デバイスとして組み込んだ固体素子を作るための基礎知見だと言って研究費を獲得していたが、分子レベルの配線がネックとなり実現には及ばなかった。1998年12月から助教授としてメンバーに加わった中村暢文先生(東京農工大学教授)はタンパク質とラマン分光の専門家で、我々と異なる専門分野から鋭い指摘をしてくれた。耐熱性タンパク質の設計にも関与し、イオン液体中ではシトクロムcが140℃でもレドックス応答を示すことを発表した16。ここでもタンパク質はか弱い材料ではないこと、また、温度は溶媒の分子運動の程度を表すので、イオン液体中の140℃はそれほど激しい分子運動の環境ではないことを述べ、論文を読んでもらうためにGraphical Abstractは共著者の賛同は得られなかったが、図3にした。
中村先生は我々が不得意な分野をカバーしてくれ、独自の研究も推進していったが、当時の3女傑(伊藤、山口、来栖)にはなかなか苦労していた。そもそも我々の研究室には強い女性が多く、研究から飲み会まで全て取り仕切っていた。我々の研究室で博士学位を取得した学生は36名だが、そのうち12名は女性だ。女性は研究職に向いているので、もっと活躍して欲しいが、社会のサポート体制が追いついていないのが残念だ。
温めると溶けにくくなる溶液との付き合いがこの頃始まった。
図3. イオン液体中のシトクロムcは140℃でも元気
8. 非接触導波路分光法
上述のPEO-修飾タンパク質の研究も進み、炭素電極上に固定したPEO-修飾シトクロムcの可視スペクトルが、活性中心の鉄イオンのレドックスに伴ってどう変化するのか調べようとしていた。炭素電極だから可視光は透過しない。と言って透明電極だけに頼ることは新規性が無いので、対象外とした。そんな折、非接触導波路分光法と言うのもがあることを知り、我が国ではシステムインスツルメンツ㈱の高橋浩三さんが専門家であることまで辿り着いた。そこで、直接測定をしてみたいと電話し、1998 年4月28日に大学院生の来栖史代さん(三菱化学)と出かけて行った。可視光が薄い石英板を全反射しながら進むときに発生するエバネッセンス波を使って吸収スペクトルを得るという方法論であった。この方法論を展開し、PEOに溶解させたPEO修飾タンパク質のスペクトル測定から始め、わずかに離れた炭素電極上に固定したシトクロムcのスペクトルも得られるようになった17,18。シトクロムcの酸化還元に伴って可視スペクトルが変化するのを見たときは感動した。
非接触導波路分光法はいろいろな展開が可能であり、来栖さんから引き継いだ藤田恭子さん(東京薬科大学専任講師)らと蛍光発光や偏光吸収も含めいろいろ楽しんだ。この辺の研究の経緯は高橋氏の論文19に詳しい。
9. PEO-塩ハイブリッド
PEO中の塩の溶解度は鎖末端のヒドロキシル基が重要な役割を果たしていることが分かった。たとえば過塩素酸リチウムの溶解において、エーテル酸素の寄与は約1.0mol/Lの溶解度分に相当し、それ以上溶解させるためには多くのヒドロキシル基が必要である20。そのために高分岐状のポリエーテルが有効だと言うことになり、側鎖に短いPEOをたくさんつけた櫛形ポリマーの提案につながった。そうこうしているうちに、末端にカルボキシル基がついたPEOをリチウム塩にし、これがリチウムイオン伝導体にならないかと考え、測定してみるとまあまあ良い伝導体であることが分かった21。イオン伝導体に関しては本学で博士学位を取得した伊藤香織さんがものすごい勢いで研究を推進していた。彼女は末端にカルボキシル基がついたPEOをリチウム塩(PEO/塩ハイブリッド)にした時に、分子量によってその物性が大きく異なることを見つけていた。即ち、分子量が数百のPEOを塩ハイブリッドにするとイオン液体になることをいち早く見つけていた(図4)。この時代にはまだ「イオン液体」と言う言葉は無く、アモルファスな塩と言う表現に留まっていた。これが溶融塩の一種であると報告したのは1998年だった22。
このPEO/塩ハイブリッドは様々な形に展開して行った。末端のアニオン構造がイオン伝導度に及ぼす効果の解析23、櫛形ポリマー誘導体、末端にカチオン構造を導入したアニオン伝導体などは面白い研究だった。富永洋一君(東京農工大学教授)はこれらのハイブリッド24について幅広く研究し、イオン伝導性ポリマー研究の世界に入って行った。

図4. 適切な分子量のポリエーテル/塩ハイブリッドはイオン液体と考えることができる
PEO/塩ハイブリッドの研究を展開している頃、イオン液体(当時はイオン性液体とも呼ばれていた)と言う言葉が聞かれるようになった。1992年に発表されたWilkes らの論文25は一部の研究者の間で認識されたが、まだ大きな流れになるようなことは無かった。前節で述べたように、PEO末端にイミダゾリウム塩を固定したハイブリッド22がイオン液体で、イオンを伝導することは既に報告していたので、今度はイオン液体そのものを高分子化してみようと言うことになり、伊藤さんがビニルイミダゾリウム塩を重合して世界で初めてイオン液体の高分子化を報告した26。イオン液体は液体の塩と言うことで興味を引いたが、「それを固体の高分子にして何が面白いんだ?」と質問された。電荷密度が高く、ガラス転移温度(Tg)の低いポリマーはとてもユニークだったので、イオン伝導体として期待できた。しかし、イオン伝導体だけでなく、非常に広い分野・領域で使われることになるとは思ってもいなかった。その後、吉澤君(藤田正博;上智大学教授)は枝の末端にイオン液体構造を持つくし型ポリマーを合成し、物性を解析27し、イオン液体ポリマーの世界に入って行った。伊藤さんはこれらの研究領域を総括する大番頭的な存在として研究室で活躍していた。イオン液体の高分子化の経緯は総説にまとめたので参考にして欲しい28。
11.Zwitterionic liquids
難燃性のイオン液体は電解質材料として期待されたが、電池などのエネルギーデバイスに利用するときは、イオンの伝導マトリックスであるイオン液体を構成するイオンが移動してしまい、目的イオンのみを伝導させることができなかった。それを解決するための研究を進め、解決策を提案した。一つは上述のイオン液体の高分子化であり、もう一つはイオン液体を構成するイオンを共有結合で結んだzwitterionic liquids29 である。吉澤君が伊藤さんたちと協力して、イオン液体をzwitterion型にしたものを合成し、そのイオン伝導性を研究した。自由度が低下するためか、イオン液体を構成するカチオンとアニオンを共有結合で結びzwitterion型にすると、融点は130℃~200℃も上昇してしまう。もはや液体とは言えない状態になってしまった。仕方なく、これに種々のリチウム塩を混合し、イオン伝導度を観測したが、当然高いイオン伝導度は認められなかった。さらに塩の種類を増やして検討していると、LiTFSI(LiTFSA)塩を添加した時に、大きなイオン伝導度が観測された29。それが、図5に示すように、TFSAアニオンがzwitterionのイミダゾリウムカチオンとイオン液体様の低Tg環境を作り、イオン移動に有利な場ができたためであることが分かった。その後、zwitterionic liquidsはいろいろな研究に使われるようになってきた30。
イオン液体関係の国際会議で、私がzwitterionic liquidsの話をしたら、会場にいた 故Ken Seddon 教授から「ヒロ、それは定義上イオン液体ではないよ。」とコメントを貰った。その後のイオン液体関係の別の国際会議で、そのことを話題にし、「それに対し私はこうコメントしました。“I don’t care.”」と言って、笑いを誘うのに使った。後年、上智大学の教授になった藤田君はオリゴエーテルを巧みに導入して液状のzwitterionic liquidsの合成に成功している31。
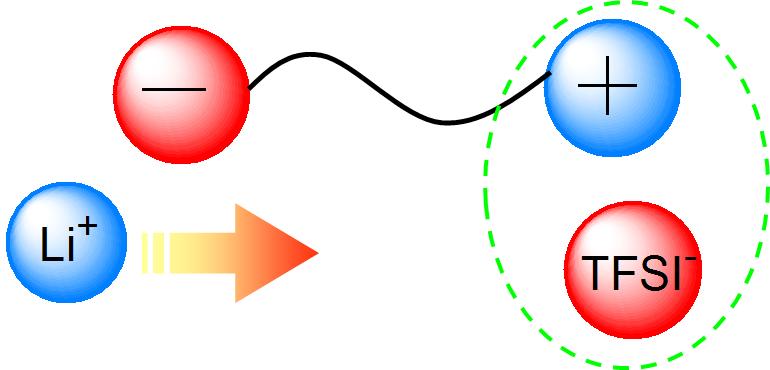
図5. Zwitterionic liquidにLiTFSA塩を加えると高イオン伝導度が得られた。
12.イオン液体の次元制御
1996年頃の科研費の全体会議(の後の懇親会)で東京大学の加藤隆史教授と「液晶とイオン伝導」というキーワードで共同研究すると面白そうだねと意気投合し、すぐに学生を派遣したりして共同研究をスタートさせた。我々の研究室からは伊藤さん率いるグループが、東大の加藤研からは大竹君(セイコーエプソン)たちが共同研究に関わり、あれこれ楽しく実験を進めた。当時はFAXでデータを送り、議論するスタイルで、ZoomもWeb 会議も無かったが、山のように積まれてゆくFAXシートを見ながら、議論したり論文案を練ったりしたのは楽しい思い出だ。図6はその一例で、日付は1998年12月16日とある。アレニウスプロットが点だけで描かれており、相転移する物質系の解析に威力を発揮した。分子集合状態をうまく制御して、イオン伝導に異方性を付与する論文32が印刷になったのが共同研究を始めて3年後の1999年だったが、その後、成果が続々と出てきた。研究を中心に様々な局面で合同イベントを開催してきた。加藤研は液晶研究では世界トップの研究を推進しており、交流を通じていろいろ刺激を受けた。我々もPEOのみならず、イオン液体にも次元制御の概念を適応し、研究を進めてきた。この共同研究は20年以上続き、たくさんの興味深い成果は50報以上の論文になっている。それらの一部は一川尚広君(東京農工大学准教授)が総説33に取りまとめている。そもそも一川君は加藤研の学生で、昔から良く知っていた。2010年の10月から研究室の助教としてメンバーに加わり、この分野の研究を一段と加速させると共に、ジャイロイド構造という新しい集合体の研究を進めている。
イオン液体の次元制御は私の大きな研究テーマの一つでもあり、液体に次元制御を適用させると何ができるがという問いに対する答えをまとめてきた。詳細は別紙34にまとめたので読んで欲しい。

図6. 加藤研との打ち合わせに使ったデータの例
13.アミノ酸イオン液体
故福元健太君が奮闘努力し、世界で初めて20種類のアミノ酸を全てイオン液体化した(図7)35。彼は吉澤君と協力して、アミノ酸をアニオンとして扱い、イミダゾリウムカチオンと組み合わせてイオン液体を作成し、新しい研究分野を開拓した。この論文は1100件以上引用され、機能イオン液体の展開に寄与した。その後、光学異性体のアミノ酸でイオン液体を作って物性を比較したり36、アミノ酸を混合してイオン液体化すると、物性が直線的には変化しない37ことを見つけたり、疎水性で低密度イオン液体38を作成したりした。この辺から複数種のアニオン間相互作用を機能に結びつける研究も進んだ。“Amino acid ionic liquids”というタイトルの総説39も500件以上引用されている。この研究から派生したものに、LCST型相転移を示すイオン液体があるが、それについては後述する。

図7. 20種類のアミノ酸イオン液体
14.思い出深い機能イオン液体
ここで、小休止の意味で、トピックス的に印象の強い機能イオン液体について紹介しておく。
14-1.中和法
当時、イオン液体は蒸気圧がほとんどないため、精製に苦労していた。そこで、簡単にイオン液体を作成する方法として、酸と塩基の中和で塩を作る方法を利用しようと言うことになり、平尾満智子さん(土屋満智子:丸善石油化学)が伊藤さんと一緒に数多くの例を検討し、簡単に液体の塩を得ることに成功した40。中和法は簡便で、研究室内でも沢山の展開につながった。この研究があったことにより、たくさんのイオン液体のモデルとでもいえる候補を数多く設計・合成できた。
14-2.DNAのイオン液体化
東京農工大学において私の所属は生命工学科だったので、周囲に細胞、酵素、遺伝子、センサーなどの言葉が氾濫していた。そこで少なからず生体物質に興味を持ち、それらとイオン伝導のクロスキーワードで何ができるが考えていた。当時、DNAを分子ワイヤーにする話があったので、DNAを電線として使ってタンパク質の酸化還元をやろうと1996年頃から研究をスタートした。DNAを被覆した電極や、DNA-修飾タンパク質41の設計などを行い、色素のインターカレーションによる伝導度の向上と電子移動の関係を調べたりしていた。後年、ビオローゲンをDNAにインターカレートさせると酸化還元反応に伴うビオローゲンの2量体形成を抑止でき、電子伝導体としても機能することを柿部剛史君(兵庫県立大学)が明らかにした42,43。
DNAとイオン液体とのコンポジットは滝沢直美さん (西村直美:東京農工大学) が精力的に研究を進め、イオン伝導性のフレキシブルDNAフィルムを作り上げた44,45。ついにはDNAのリン酸残基の対カチオンとしてイミダゾリウムカチオンを導入し、イオン液体で包まれたようなDNAを作成した46。同時期に、外側をイオン液体化できるのならば内側もできるだろう!と考えた。核酸塩基を眺めてみるとπ共役したヘテロ環であり、プロトン付加させればカチオンになるのでは?と考えた。まず、低分子モデルからと言うことで、核酸塩基を購入し、中和法でTFSA塩にしてみると、シトシン塩が液体で得られた47。核酸塩基のプロトン付加は多段のステップがあり、構造的な議論が難しいが、その辺は他の研究者に任せ、シトシンのTFSA塩が液体になったことをもとに、DNAのらせん内部の塩基のイオン液体化を試みた。核酸塩基間の相補的な水素結合は崩れるので、二重らせん構造は壊れる。TFSA導入DNAは疎水性だったが、BF4 導入DNAは水溶性だったので、イオン伝導性フィルムにすることができた。

図8. イオン伝導性DNAフィルム
14-3.高屈折率イオン液体
面白いイオン液体として、高屈折率のイオン液体を作った。すでに、赤外領域で高屈折率のイオン液体についてはSeddonらの報告があったので、可視光領域で高屈折率を示すイオン液体をターゲットにした。ちょうど、研究室ではイオン液体の極性の議論が盛んになされており、Kamlet-Taft Parametersを多くの学生が評価していた。一川君の指導の下、嘉山遥子さんがそれらと屈折率の相関解明に挑戦し、π*値と呼ばれるパラメターと屈折率の間に相関があることを明らかにし(図9)、それをもとに屈折率が1.6を超えるイオン液体を提案・合成した48。
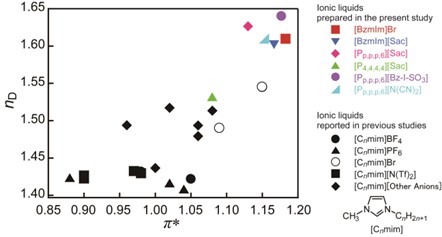
図9. イオン液体のπ*値と屈折率の相関 略称の説明は省略
14-4.生体由来イオン液体
イオン液体は様々な用途に使われ、バイオ分野にも進出してきた。それに合わせてイオン液体の毒性に関心が集まるようになってきた。そもそも塩なので、体内に入れば浸透圧が変わるので、生物にとっては毒である。食塩も大量に摂取すれば死に至る。体内に少量添加して機能化を目指す目的の研究が増えてきたので、我々も低毒性のイオン液体には興味があった。しかし、毒性検査などは専門的な知識と装置が必要なので、発想を変えることにした。つまり、体内に存在する成分を組み合わせてイオン液体が作れないか?という課題を設定した。深谷幸信君(東京農工大学)を中心として、構成イオンの候補を探索した。体内には数多くのカルボン酸が存在する。一方、イオン液体形成に有利と思われる構造を有するカチオンの多くは毒性が高く、殺菌剤などに使われている位であったため、コリンに注目した。当時、研究室では藤田さんがコリニウム・リン酸二水素塩と少量の水を混合させて得られる水和イオン液体の研究(後述)を進めていたので、コリンはなじみ深い材料であった。コリニウムクロライドは安価で簡単に入手できるので、これをアニオン交換して、一連のカルボン酸塩とした。精製後、物性を調べると室温で液体の塩が見つかった。カルボン酸塩は一般に水素結合受容性が強い(前述のKamlet-Taft Parameters の中のβ値が大きい)ので、ここで得られたいくつかの塩も高極性であった49。具体的な毒性は評価しなかったが、生体由来イオン液体の考え方は広く受け入れられた。
14-5.アゾリウム・アゾレート型イオン液体
C、H、Nの元素だけでできたイオン液体を作った。荻原 航君(日産自動車)は吉沢君と協力して、アゾールイオンだけで構成されたイオン液体を作成した50。アルキルイミダゾリウムトリアゾレート(あるいはテトラゾレート)は興味深いイオン液体となったが、爆発性のため、それ以降研究は進めなかった。その後、米国のRogersらが燃料として類似のイオン液体を報告したこともあり、アゾリウム・アゾレートはいくつか研究例が出てきた。が、研究室を爆破したくなかったので、この研究は取りやめた。
14-6.ホウ素を使った機能材料
京都大学の中條研で博士学位を取得した松見紀佳君(北陸先端科学技術大学院大学教授)が我々の研究室に助教として2000年から加わった。彼はホウ素化学のプロで、イオン伝導とホウ素のクロスキーワードで面白い研究を進めた。ホウ素の空のp軌道を使ってアニオンをトラップし、カチオン伝導体やカチオン伝導性高分子を設計したり、新しいイオン液体の設計に携わったりした51-54。彼はなかなかのいたずら好きで、被害?にあった学生は多かったが、研究成果のみならず、研究室の雰囲気作りにも大いに貢献してくれた。
14-7.HPILC
記載が前後してしまうが、次項で述べるセルロースを溶かすイオン液体の研究から派生したものにHigh Performance Ionic Liquid Chromatography の研究がある。イオン液体を溶媒としてHPLC分析をしてみよう、と研究室内の議論で発案した。当然、高粘度であるイオン液体を溶媒として使用することは、HPLCを使っている研究者から見ると、ありえない提案である。しかし、我々としてはイオン液体に溶解した高分子の状態分析を「溶けたまま」行いたいという強い欲求があった。耐圧ポンプを使い、必要ならばカラムを加熱してでもいいからイオン液体溶液の分析をしようと決めた。黒田浩介君(金沢大学准教授)と深谷君が苦労してシステムを作り上げた。平均分子量が既知のプルランを溶解したイオン液体を流し、屈折率変化で分析してみると、分子量に対応した流出時間のシフトが観測できた。このときは嬉しかった。早速投稿し、High Performance “Ionic Liquid” Chromatography というタイトルの論文が印刷になった55。黒田君は、これをベースにいくつかの展開を図り、学位を取得した。
このほかにもたくさんの研究が思い出されるが、紙面の都合(実は執筆時間の都合)により、省略する。
15.木を溶かすイオン液体
16.水和イオン液体
2000年頃からゴムとイオン液体のコンポジットを作り、フレキシブルイオン伝導フィルムを作ることを始めた。更に対象は多糖類やDNAにまで拡がり、様々な高分子とイオン液体の相互作用研究や、コンポジット作成を多くの学生が挑戦した。特に多糖類については様々なものに挑戦した。コンポジットを作るためには、溶解させる必要がある。そこで、種々の多糖類の溶解度を様々なイオン液体中でチェックした。2005年の日本化学会の春季年会で、でんぷんにイオン液体構造を導入して、イオン伝導体にする研究を西村直美さんが発表している。学会等で「イオン液体を使えばセルロースを溶かすことはそう難しくない。ちょっと加熱すれば溶かせる。」と発表していたら、2007年6月1日に森林総研の山田竜彦博士が農水省の偉い人と一緒に研究室に来られ、「木材を溶かすことができるって本当ですか?」と膝を乗り出して聞いてきた。セルロースを溶かすことは実験結果が出ていたが、「将来、木を溶かすこともできるだろう。」という発言の「将来」と「だろう」を除いて理解されていたようで、少々説明をしたが、説明しているうちに、木材の構成要素の一つのリグニン(3次元ネットワークを構築している)の扱い次第では木を溶かすというのも不可能ではなさそうだ、と思うようになった。この研究はNEDOに申請したものは通らなかったが、日産財団から支援して貰えることになった。深谷君が中心となって研究を進め、2008年にはセルロースを溶かすイオン液体に必要なアニオンの要件に関する論文56が印刷になった。これは結構注目され、800件ほどの論文に引用されている。2007年の訪問が契機となり、森林総研の山田竜彦博士との付き合いが始まり、農水省のプロジェクトや内閣府のSIPプロジェクトにも参加できた。その後もセルロースを溶かすイオン液体の研究は進み、多くの論文が生まれた57。
セルロースを溶かすイオン液体を作成するためにはアニオンの選択が重要であることは上述の論文でも明らかなように、研究室では常識になっていた。クロライド塩は一般に水素結合受容性が大きいことが分かっていたが、イオン半径が小さいので静電的な相互作用が強いため、結果的にクロライド塩の融点は高いことが欠点であった。世界的にはクロライド塩を加熱して溶融させてからセルロースの溶媒として使っていた。水雲智信君(広島大学)が松見君と協力し、イミダゾリウム環にアリル基を導入して世界で初めて空気中で安定な液状クロライド塩を作製した。我々がもたもたしている間に、これを用いてセルロースを溶かしたという論文が出た。
セルロースの非加熱溶解にこだわっていた我々は、新しいアニオンについて常に議論していた。ある日、研究発表会でCl-の代わりにOH-を使ってみたらどうだ?と阿部 充君(産業技術総合研究所)に言った。「ただのアルカリじゃないですか!」と言われたが、とにかく、イオン液体のアニオンをOH-にしてみろ、とやんわりと指示。色々調べてみると、北興化学工業㈱がテトラブチルフォスフォニウム水酸化物水溶液を作っていることを知った。40%の水を含む溶液を何とか入手し、セルロース粉末を添加してみると、加熱もしないのにスイスイと溶けてゆく。どんどん量を増やしてみたら、終濃度が20%になるようにセルロースを加えても5分程度で完全に溶解した。加熱しないでこんなに溶けるなんて、と驚いた。早速、データをそろえ、周辺データも取り揃えて論文58とした。この発見の後、テトラブチルフォスフォニウム水酸化物水溶液誘導体も含めた一連の研究が進んだ。当然、これはイオン液体ではない。学会でもその点を指摘されることがあったが、"I don't care."で済ませた。セルロースが簡単に溶ければいいじゃないか!
研究室で博士学位を取得し、オーストラリア、Monash大学のMacFarlane教授のところで研究を推進していた藤田さんが我々の研究室に学振RPDで戻ってきた。オーストラリアでコリニウムリン酸二水素塩に少量の水を加えたものがタンパク質をよく溶かすことを見つけ、その研究をさらに展開した。
イオン液体に少量の水が混入していると、粘度をはじめとして諸物性が大きく変わることは良く知られていた。そのため、イオン液体の本当の物性を測定するためには混入している水の含量を徹底的に低減させることが必要であった。我々はそれを逆手に取り、水をちょっと足してイオン液体の物性を制御しようとしていた。藤田さんが中心となり、少量の水を足したイオン液体を「水和イオン液体」と呼んで、精力的に研究を進めた。この水和イオン液体中ではすべての水分子はイオンと直接相互作用しており、自由水は無い。後に、この水和イオン液体が細胞膜の表面と類似の環境であることを主張し、生命の起源に関係しているのでは、と第4回イオン液体国際会議で発表59した時は会場が満員になった。水和イオン液体中ではいくつかのタンパク質が機能を保持できる。これを使えばバイオ燃料電池ができる可能性があることを示すために、セロビオースを酸化させ、電子を取り出すことに成功した(図10)60。その後も水和イオン液体の研究は推進され、タンパク質の再構成ができることを藤田さんが見つけ、液体シャペロンと名付けた61。大腸菌でタンパク質を産生させるときに大部分はアグリゲートとして得られるが、それらを水和イオン液体に溶かすだけで再構成できるようになりそうだ。他にも様々な展開が期待できる。
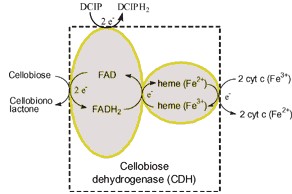
図10. セロビオースの酸化反応(模式)
17.LCST型相転移
前述のアミノ酸イオン液体を福元君が研究中に、アミノ酸をより疎水性にするためにアミノ基を修飾し、トリフロロメタンスルホニル化アミノ酸を作った。これをテトラブチルフォスフォニウムカチオンと組み合わせて疎水性イオン液体を作成した。このイオン液体に水を加えると、温度に応じて水との親和性が大きく変わることを福元君が見つけた(図11)62。色素で着色してあるイオン液体に水を加えると、25℃では相分離しているが、これを徐々に冷却して22℃にすると、完全に相溶する。25℃に戻せば再度相分離する。このように2つの液体の親和性(溶解性)が加熱すると低下し、冷却すると向上するような現象を下限臨界溶解温度(LCST)型相転移と言う。水とイオン液体の組み合わせでは我々が初めて見つけたが、わずか3℃の変化でここまで大きな相転移を示す系は珍しい。この研究を引き継いだ河野雄樹君(産業技術総合研究所)がLCST転移前後で水溶性タンパク質の溶解性が変わることを見つけた63。図12に示すように、25℃においてイオン液体の上にシトクロムcが溶けた水溶液を静かに加え(a)、温度を20℃に冷却すると、系は均一溶液になる(b)。これを再び25℃にするとシトクロムcが全てイオン液体相に移ってしまった(c)。この結果を河野君が持ってきたときには信じられなかった。目の前で実験を再度行ってもらい、認めざるを得なくなった。どうしてこうなるのか?と言う問いに答えが出たのはしばらくたってからだった。タンパク質の溶解性に及ぼす塩濃度の効果は、塩析や塩溶として知られているが、相転移後の水相のイオン液体濃度がシトクロムcがちょうど塩析する値であった。それに対し、イオン液体相は水を含み、塩溶の条件になっていたことが分かった。

図11. 水と混合後LCST型の相転移を示すイオン液体の例
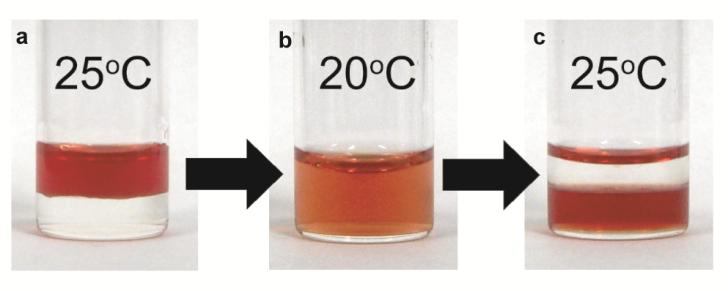
図12. シトクロムcの溶存状態に及ぼす相転移の効果
一旦、プロトコルが得られれば、水と混合後にLCST型の相転移を示すイオン液体の設計は容易になる65。高分子化イオン液体でも転移温度前後で水との親和性が大きく変わるので、いろいろな展開が可能となった66。
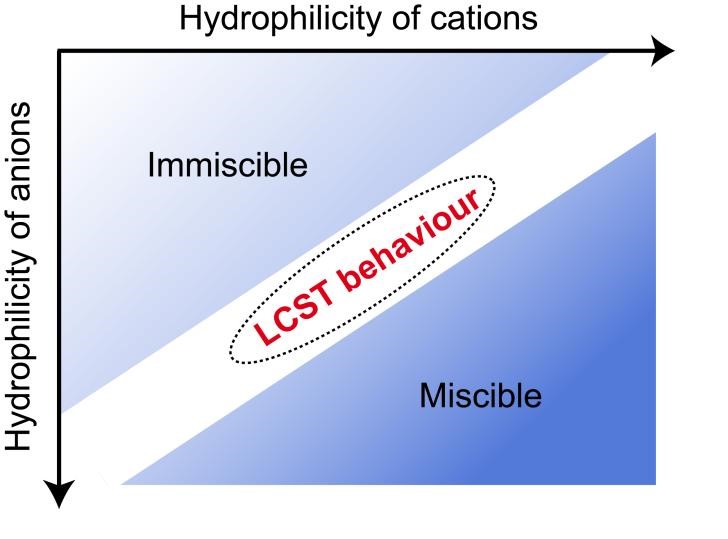
図13. 水と混合後LCST型の相転移を示すイオン液体の例
このゲルの特性を利用すれば、親水性と疎水性の環境を必要とする2段の触媒反応を進行させることもできる69。

図14. 温度変化に応じて水を吸脱着するイオン液体ゲル
18.終わりに
このように項目別にイオン液体関連の研究を並べてみると、実はそれぞれの相関が見えてこない。それぞれの研究は決して独立しているわけではなく、発展的に生まれたものもあるし、必要となって新しいテーマに育ったものもある。記載が時系列に沿っていない部分があるが、ご容赦願いたい。
今回は紙面が限られているので、詳細は述べないが、ここに記した研究が、個性的なものであると思って頂けたら嬉しい限りである。しかし、個性的な研究を進めることは実に難しいものである。最後に、東京農工大学で30年以上の教育・研究生活を共に行ってくれたスタッフ、学生諸君に心から感謝する。
引用文献
- H. Ohno, Y. Maeda and E. Tsuchida, Biochim. Biophys. Acta, 642, 27 (1981)
- K. Honda, Y. Maeda, S. Sasakawa, H. Ohno and E. Tsuchida, Biochem. Biophys. Res. Commun., 100, 442 (1981)
- H. Ohno, N. Shimidzu, E. Tsuchida, S. Sasakawa, and K. Honda, Biochim. Biophys. Acta., 649, 221 (1981)
- H. Ohno, H. Takinishi and E. Tsuchida, Makromol. Chem., Rapid Commun., 2, 511 (1981)
- H. Ohno, M. Shibayama and E. Tsuchida, Makromol. Chem., 184, 1017 (1983)
- E. Tsuchida, H. Ohno and K. Tsunemi, Electrochim. Acta, 28, 591 (1983)
- N. Kobayashi, R. Hirohashi, H. Ohno, and E. Tsuchida, Solid State Ionics, 40/41, 491 (1990)
- H. Ohno, S. Takeoka and E. Tsuchida, Polym. Bull., 14, 487 (1985)
- H. Ohno, Y. Ogata and E. Tsuchida, Macromolecules, 20, 929 (1987)
- H. Ohno, Y. Inoue, and P. Wang, Solid State Ionics, 62, 257 (1993)
- 大野弘幸、伊藤香織、松本晃治、日本化学会誌、301 (1993)
- H. Ohno and K. Ito, Polymer, 34, 4171 (1993)
- 大野弘幸、山口夏江、化学、47, 360 (1992)
- F. Kurusu, N.Y. Kawahara, and H. Ohno, Solid State Ionics, 86-88, 337 (1996)
- H. Ohno and N. Yamaguchi, Bioconjugate Chem., 5, 379 (1994)
- K. Tamura, N. Nakamura, and H. Ohno, Biotech. Bioeng., 109, 729 (2012).
- H. Ohno, K. Fukuda, and F. Kurusu, Chem. Lett., 76 (2000)
- 大野弘幸、藤田恭子、日本接着学会誌、38, 306 (2002)
- 高橋浩三、電気化学および工業物理化学、 72, 123 (2004)
- 大野弘幸、王 璞、日本化学会誌、1588 (1991)
- H. Ohno and K. Ito, Polymer, 36, 891 (1995)
- H. Ohno, Y. Nakai, and K. Ito, Chem. Lett., 15 (1998) <
- K. Ito, N. Nishina, Y. Tominaga, and H. Ohno, Solid State Ionics, 86-88, 325 (1996)
- Y. Tominaga and H. Ohno, Solid State Ionics, 124, 323 (1999)
- J.S.Wilkes, M.J. Zawarotko, J. Chem. Soc., Chem. Commun., 965 (1992)
- H. Ohno and K. Ito, Chem. Lett., 751 (1998)
- M. Yoshizawa and H. Ohno, Chem. Lett., 889 (1999)
- N. Nishimura and H. Ohno, Polymer, 55, 3289 (2014)
- M. Yoshizawa, M. Hirao, K. I-Akita, and H. Ohno, J. Mater. Chem., 11, 1057 (2001)
- H. Ohno, M. Yoshizawa-Fujita, and Y. Kohno, Phys.Chem.Chem.Phys., 20, 10978 (2018)
- M. Yoshizawa-Fujita, T. Tamura, Y. Takeoka, and M. Rikukawa, Chem. Commun. 47, 2345 (2011)
- T. Ohtake, K. Ito, N. Nishina, H. Kihara, H. Ohno, and T. Kato, Polymer J., 31, 1155 (1999)
- 一川尚広、大野弘幸、高分子、65, 68 (2016)
- T. Ichikawa, T. Kato, and H. Ohno, Chem. Commun., 55, 8205 (2019)
- K. Fukumoto, M. Yoshizawa and H. Ohno, J. Amer. Chem. Soc., 127, 2398 (2005)
- K. Fukumoto, Y. Kohno, and H. Ohno, Chem. Lett., 35, 1252 (2006)
- J. Kagimoto, K. Noguchi, K. Murata, K. Fukumoto, N. Nakamura, and H. Ohno, Chem Lett., 37, 1026 (2008)
- J. Kagimoto, S. Taguchi, K. Fukumoto, and H. Ohno, J. Molecular Liq., 153, 133 (2010)
- H. Ohno and K. Fukumoto, Acc. Chem. Res., 40,1122 (2007)
- M. Hirao, H. Sugimoto, and H. Ohno, J. Electrochem. Soc., 147, 4168 (2000)
- K. Muneyasu, N.Y. Kawahara, and H. Ohno, Solid State Ionics, 113-115, 167 (1998)
- T. Kakibe and H. Ohno, Chem. Commun., 377 (2008)
- T. Kakibe and H. Ohno, J. Materials Chem., 19, 4960 (2009)
- H. Ohno and N. Takizawa, Chem. Lett., 642 (2000)
- H. Ohno and N. Nishimura, J. Electrochem. Soc., 148, E168 (2001)
- N. Nishimura, Y. Nomura, N. Nakamura, and H. Ohno, Biomaterials, 26, 5558 (2005)
- 大野弘幸、化学と教育、52, 174 (2004)
- Y. Kayama, T. Ichikawa, and H. Ohno, Chem. Comm., 50, 14790 (2014)
- Y. Fukaya, Y. Iizuka, K. Sekikawa, and H. Ohno, Green Chem., 9, 1155 (2007)
- W. Ogihara, M. Yoshizawa, and H. Ohno, Chem. Lett., 33, 1022 (2004)
- N. Matsumi, K. Sugai, and H. Ohno, Macromolecules, 35, 5731 (2002)
- N. Matsumi, K. Sugai, and H. Ohno, Macromolecules, 36, 2321 (2003)
- N. Matsumi, M. Miyake, and H. Ohno, Chem. Commun., 2852 (2004)
- N. Matsumi, A. Mori, K. Sakamoto and H. Ohno, Chem. Commun., 4557 (2005)
- Y. Fukaya, A. Tsukamoto, K. Kuroda, and H. Ohno,Chem. Commun., 47, 1994 (2011).
- Y. Fukaya, K. Hayashi, M. Wada, and H. Ohno, Green Chem., 10, 44 (2008)
- H. Ohno and Y. Fukaya, Chem. Lett., 38,2 (2009)
- M. Abe, Y. Fukaya, and H. Ohno, Chem. Commun., 48, 1808 (2012)
- “Did ionic liquids support origin of life?” (#53) H. Ohno and K. Fujita, 4th Congress on Ionic Liquids (COIL-4) 2011年6月16日, Washington DC, USA
- K. Fujita, N. Nakamura, K. Igarashi, M. Samejima and H. Ohno, Green Chem., 11, 351 (2009)
- K. Fujita, M. Kajiyama, Y. Liu, N. Nakamura, and H. Ohno, Chem. Comm., 52, 13491 (2016)
- K. Fukumoto and H. Ohno, Angew. Chem. Int. Ed., 46, 1852 (2007)
- Kohno, S. Saita, K. Murata, N. Nakamura, and H. Ohno, Polym. Chem., 2, 862 (2011)
- Y. Kohno and H. Ohno, Physical Chemistry Chemical Physics, 14, 5063 (2012)
- Y. Kohno, H. Arai, S. Saita and H. Ohno, Australian J. Chem., 64, 1560 (2011)
- Y. Kohno and H. Ohno, Chem. Commun., 48, 7119 (2012)
- Y. Deguchi, Y. Kohno, and H. Ohno, Australian J. Chem., 67, 1666 (2014)
- Y. Deguchi, Y. Kohno, and H. Ohno, Chem. Comm., 51, 9287 (2015)
- A. Okafuji, Y. Kohno, N. Nakamura, and H. Ohno, Polymer, 134, 20 (2018)
